眾所周知,肥胖是導致2型糖尿病的重大風險因素。然而在薩摩亞、毛利人等人群中,肥胖率居于全球前列,但很少患2型糖尿病。調查發(fā)現(xiàn),這些肥胖人群攜帶特有的CREB 3 regulatory factor基因變體, 即CREBRFR457Q。培育能夠模擬表型相似實驗動物模型,闡明其背后的機制,將為研發(fā)降低肥胖人群患糖尿病發(fā)生幾率的藥物提供有效靶標。國外學者建立了與人CREBRFR457Q同源點突變的小鼠模型,但小鼠模型并沒有表現(xiàn)出肥胖表型、代謝相關指標的異常以及對2型糖尿病的保護作用。由于豬脂質代謝和胰島結構等與人更為相似,本研究利用基因編輯和體細胞克隆技術,成功地培育了CREBRFR457Q點突變豬模型,并獲得了可育后代。
CREBRFR457Q點突變豬表現(xiàn)出肥胖表型,其體重、腹圍以及總體脂肪含量均高于野生型豬,并且脂肪積累主要在皮下,內(nèi)臟脂肪積累不顯著。與野生型的脂肪組織相比,點突變豬脂肪細胞數(shù)量多,體積小。體外脂肪分化實驗也表明CREBRFR457Q變體促進前脂肪細胞分化。CREBRFR457Q導致的肥胖是由脂肪細胞數(shù)量增加(增生)而不是體積增大(過度增大)引起的,CREBRFR457Q點突變導致的肥胖在某種程度上是保護肥胖。血液生化分析表明該點突變在維持正常的胰島素敏感性的基礎上,上調了血液中的胰島素水平。課題組進一步通過氧化水平的監(jiān)測,發(fā)現(xiàn)該點突變能降低脂肪組織中氧化代謝能力、增強抗氧化能力,減少ROS的產(chǎn)生,從而降低氧化應激水平,以及由此帶來的胰島素抵抗等反應。本研究初步揭示了該點突變通過促進脂肪細胞生成導肥胖癥,而通過降低氧化代謝、維持正常的胰島素敏感性降低2型糖尿病風險的機制,為預防肥胖人群罹患糖尿病提供了新的思路。
該論文共同通訊作者為廣州健康院樊娜娜副研究員和吳東海研究員,廣州健康院的博士生李瑩瑩、陳晃耀、博士后汪海、健康院和安徽大學聯(lián)合培養(yǎng)碩士生廖媛為共同第一作者。該研究得到了廣東省科技計劃、國家重點研發(fā)計劃、中科院先導計劃、廣州市科技計劃等多個項目的支持。
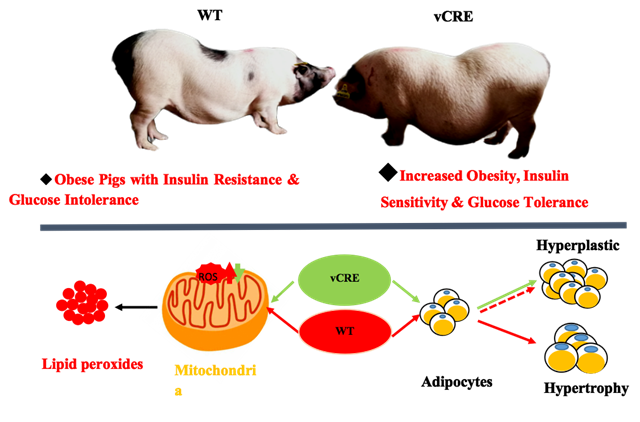
CREBRFR457Q點突變豬促進肥胖降低2型糖尿病的作用機制示意圖
附件下載:


