近日,中國科學(xué)院南海海洋研究所張長生研究員團隊和廈門大學(xué)王斌舉教授團隊合作在氮雜蒽醌類海洋多環(huán)天然產(chǎn)物Deoxynybomycin(DNM)和Nybomycin(NM)生物合成與酶反應(yīng)機制研究方面取得新進(jìn)展,相關(guān)成果 “Deciphering Deoxynybomycin Biosynthesis Reveals Fe(II)/ -Ketoglutarate Dependent DioxygenaseCatalyzed Oxazoline Ring Formation and Decomposition”在線發(fā)表于Journal of the American Chemical Society (《美國化學(xué)會志》)。博士后劉凱,博士張光濤、張錦巖(廈門大學(xué))為共同第一作者,張長生、王斌舉與張光濤為共同通訊作者。
惡唑啉是天然藥物中的重要活性基團,在有機合成小分子活性化物結(jié)構(gòu)衍生和修飾中有著廣泛應(yīng)用。2-惡唑啉環(huán)是自然界中常見的結(jié)構(gòu)形式,其在非核糖體肽、核糖體肽和苯并惡唑類天然產(chǎn)物中的生物合成途徑已經(jīng)闡明。抗生素DNM和NM是自然界中罕見的含有4-惡唑啉基團的氮雜蒽醌類化合物。DNM具有顯著抗革蘭氏陽性菌活性,也是開發(fā)抗革蘭氏陰性菌的藥物先導(dǎo)化合物,其作用機制是與DNA 型拓?fù)洚悩?gòu)酶靶向結(jié)合,阻礙細(xì)菌DNA合成而發(fā)揮抗菌作用。DNM中的4-惡唑啉環(huán)是關(guān)鍵藥效團,但其生物合成機制一直是未解之謎,限制了對這類活性氮雜蒽醌天然產(chǎn)物的深度挖掘和開發(fā)利用。
研究團隊早期從南海深海沉積物來源的假諾卡氏菌(Pseudonocardia antitumoralis SCSIO 01299,張偲院士和田新朋研究員提供)分離發(fā)現(xiàn)了氮雜蒽醌類多環(huán)天然產(chǎn)物脫氧苯醌(Deoxynyboquinone,DNQ)(Mar Drugs, 2011,9:1428-1439)。近期,與澳門大學(xué)副教授余華合作揭示了DNQ的抗炎活性靶點與作用機理,發(fā)現(xiàn)DNQ可靶向烷基化修飾信號通路(Keap1-Nrf2-ARE)中Keap1上的關(guān)鍵位點Cys489,促使Keap1泛素化,并釋放Nrf2進(jìn)入細(xì)胞核激活下游抗炎效應(yīng)因子的表達(dá),從而發(fā)揮顯著的抗炎活性(J. Pharm. Anal. 2023, doi:10.1016/j.jpha.2023.07.009)。
DNM與DNQ擁有相似的三環(huán)氮雜蒽醌線性骨架結(jié)構(gòu),可能具有相同的生源途徑。本研究基于生物信息學(xué)分析定位了菌株SCSIO 01299和Embleya hyaline NBRC 13850(DNM產(chǎn)生菌)基因組中DNQ(dnq)和DNM(dnm)的生物合成基因簇(圖1),進(jìn)一步通過體內(nèi)遺傳與體外生化實驗,發(fā)現(xiàn)了二者生物合成途徑中的共同中間體5(圖2),闡明了甲基轉(zhuǎn)移酶DnmS負(fù)責(zé)DNQ和DNM氮甲基化后修飾,兩個同源的Fe(II)/ -KG依賴型雙加氧酶DnmT和DnmU分別負(fù)責(zé)DNM中4-惡唑啉環(huán)的形成和C-12位的羥基化(圖2)。
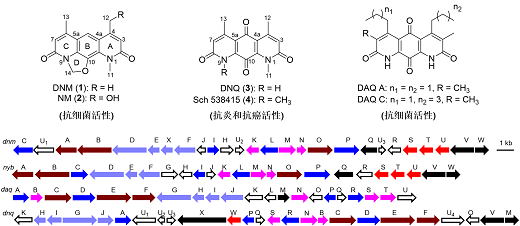
圖1. 氮雜蒽醌類天然產(chǎn)物與其生物合成基因簇
在進(jìn)行體外酶反應(yīng)研究時,研究團隊意外發(fā)現(xiàn)DnmT既能催化惡唑啉環(huán)的形成產(chǎn)生DNM,也能催化DNM中惡唑啉環(huán)的開環(huán)和脫N-甲基,最終形成中間體5,從而逆轉(zhuǎn)DNM的生物合成。為闡釋DnmT催化惡唑啉成環(huán)與開環(huán)的酶學(xué)基礎(chǔ),研究團隊基于酶蛋白建模、點突變以及分子動力學(xué)(MD)模擬和量子力學(xué)/分子力學(xué)(QM/MM)多尺度計算化學(xué)等方法詳細(xì)解析了DnmT催化成環(huán)、開環(huán)和脫甲基反應(yīng)的新穎酶學(xué)機制,同時通過體外實驗捕捉到反應(yīng)中間體14,進(jìn)一步佐證了該反應(yīng)機理的合理性(圖2)。
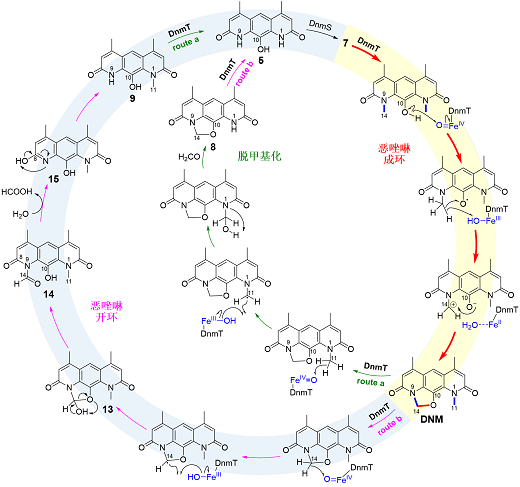
圖2. Fe(II)/ -KG依賴型雙加氧酶DnmT催化惡唑啉成環(huán)、開環(huán)和脫甲基化反應(yīng)的機制
此外,研究團隊還初步探索了DnmT催化多種反應(yīng)的生物學(xué)意義。進(jìn)一步發(fā)現(xiàn),在野生菌株中,絕大部分DNM被分泌至胞外,而胞內(nèi)含量較少;活性評估顯示,DNM對革蘭氏陽性菌的抑菌活性顯著強于NM及其它中間體和副產(chǎn)物。由此,研究團隊推測,DnmT催化惡唑啉成環(huán)產(chǎn)生DNM并釋放到環(huán)境中,殺死自己的競爭者,提升自身的生存能力;而催化惡唑啉開環(huán)和脫甲基可能是為了控制胞內(nèi)DNM的濃度,減少對細(xì)菌自身的毒性,這一假設(shè)有待進(jìn)一步的深入研究證實。
綜上所述,本研究解析了抗生素DNM中罕見4-惡唑啉藥效團的合成途徑,并利用酶學(xué)和計算化學(xué)等方法揭示了新穎多功能Fe(II)/ -KG依賴型雙加氧酶DnmT催化惡唑啉成環(huán)、開環(huán)和脫甲基化的酶學(xué)機制,為Fe(II)/ -KG依賴型雙加氧酶在天然產(chǎn)物生物合成中的功能多樣性以及其可能的生物學(xué)意義提供了新見解,同時也為活性氮雜蒽醌類天然產(chǎn)物的基因組挖掘提供了重要科學(xué)依據(jù)。
上述研究工作得到了國家自然科學(xué)基金、廣東省海洋經(jīng)濟發(fā)展(海洋六大產(chǎn)業(yè))專項資金、海南省重大科技計劃和中國科學(xué)院王寬誠率先人才計劃“盧嘉錫國際團隊項目”等的資助。
相關(guān)論文信息:1、Kai Liu#, Jinyan Zhang#, Guangtao Zhang#,*, Liping Zhang, Zhen Meng, Liang Ma, Wenjun Zhang, Weiliang Xiong, Yiguang Zhu, Binju Wang*, Changsheng Zhang*. Deciphering deoxynybomycin biosynthesis reveals Fe(II)/ -ketoglutarate-dependent dioxygenase-catalyzed oxazoline ring formation and decomposition. J. Am. Chem. Soc. 2023. https://doi.org/10.1021/jacs.3c11772
2、Ke-Gang Linghu, Tian Zhang, Guangtao Zhang, Peng Lv, Wenjun Zhang, Guanding Zhao, Shihang Xiong, Qiushuo Ma, Mingming Zhao, Meiwan Chen, Yuanjia Hu, Changsheng Zhang*, Hua Yu*. Small molecule deoxynyboquinone triggers alkylation and ubiquitination of Keap1 at Cys489 on Kelch domain for Nrf2 activation and inflammatory therapy. J. Pharm. Anal. 2023. doi: 10.1016/j.jpha.2023.07.009
附件下載:


