近期,中國科學(xué)院南海海洋研究所熱帶海洋生物資源與生態(tài)重點(diǎn)實(shí)驗室(LMB)/廣東省海洋藥物重點(diǎn)實(shí)驗室(LMM)閆巖研究員團隊完成了對真菌來(lái)源的quadrane新骨架倍半萜terrecyclic acid的生物合成研究,成果發(fā)表在英國皇家化學(xué)會(huì )旗艦期刊《Chemical Science》上,文章被該刊評為每周亮點(diǎn)論文和2024熱點(diǎn)論文。
倍半萜是萜類(lèi)化合物中占比最多的一種,分子中含15個(gè)碳原子,由三個(gè)異戊二烯單元組成鏈狀、環(huán)狀等多種骨架結構,分布于植物、昆蟲(chóng)、微生物等生物中,具有廣泛的生物活性,是醫藥、食品和化妝品研發(fā)的重要源泉。Terrecyclic acid是一類(lèi)由環(huán)戊烷駢雙環(huán)辛烷組合而成的quadrane倍半萜骨架,經(jīng)過(guò)氧化后修飾而成的一類(lèi)具有抗菌、抗腫瘤活性天然產(chǎn)物。該類(lèi)化合物最早發(fā)現于土曲霉,后又相繼從不同來(lái)源的真菌和柳珊瑚中發(fā)現(如圖1)。

圖1?來(lái)自真菌(A)和柳珊瑚(B)的天然quadrane倍半萜
由于quadrane骨架的特殊結構與良好的生物學(xué)活性,其制備方法的研究受到廣泛關(guān)注,其中合成化學(xué)家先后開(kāi)發(fā)出20余條合成路線(xiàn)。然而由于該類(lèi)化合物特殊的結構和成環(huán)方式,使得其化學(xué)合成步驟多,產(chǎn)率較低,在一定程度阻礙了先導藥物的開(kāi)發(fā)。通過(guò)合成生物學(xué)方法大量制備quadrane類(lèi)天然產(chǎn)物,是解決這一問(wèn)題的有效策略。同位素示蹤實(shí)驗表明,quadrane骨架的生物合成可能經(jīng)歷了兩種完全不同的途徑,即Hirota途徑和Coates途徑。盡管計算化學(xué)研究表明后者的可能性更高,但quadrane骨架的生物合成基因與其形成的確切酶學(xué)機制仍有待證實(shí)(路徑圖1)。
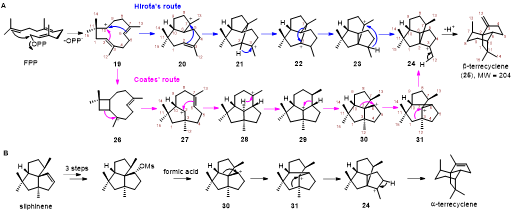
路徑圖1?推測的?β-terrecyclene形成途徑. (A) Hirota途徑?(藍色)和Coates分別由FPP生成的β-terrecyclene。(B) Coates重排形成的 α-terrecyclene。
閆巖研究員團隊通過(guò)對真菌基因組的挖掘,發(fā)現了該類(lèi)化合物的生物合成基因簇ter,包括一個(gè)萜類(lèi)環(huán)化酶(terpene cyclase,TC)即terA、一個(gè)P450氧化基因(terB)、一個(gè)短鏈脫氫基因(terC)和一個(gè)主要協(xié)同轉運因子超家族基因(terD),如圖2A。通過(guò)異源表達、體內喂養、體外酶反應等研究,驗證了基因簇中各基因的功能(圖2B-2E),證實(shí)了其生物合成途徑:即在環(huán)化酶TerA的作用下催化FPP產(chǎn)生化合物25,進(jìn)而產(chǎn)物25被P450酶TerB羥化和羧基化產(chǎn)生化合物32,最后32被脫氫酶TerC催化形成終產(chǎn)物2,如圖2F。
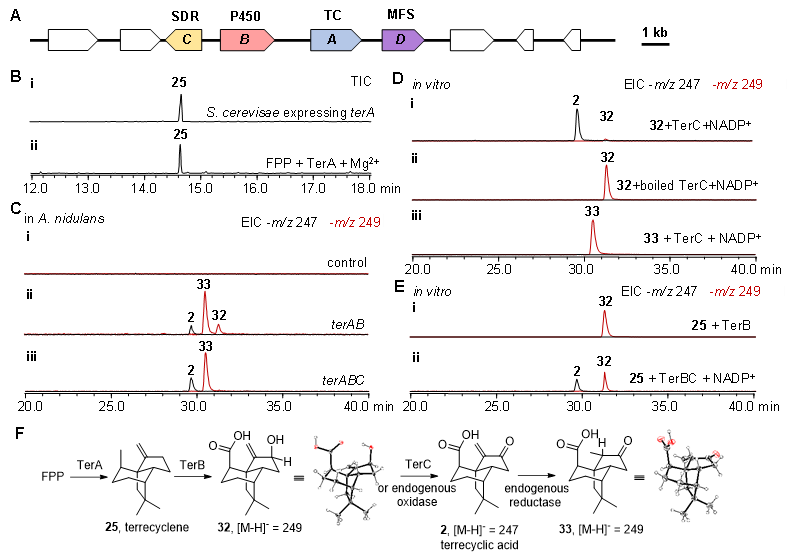
圖2?抗腫瘤倍半萜terrecyclic acid的生物合成途徑解析?(A)Terrecyclic acid的生物合成基因簇;(B)蛋白TerA在酵母S. cerevisae中的異源表達(i)和體外反應(ii);(C)基因簇ter在A(yíng). nidulans中的異源表達:(i)A. nidulans的空白對照,(ii)基因terAB在A(yíng). nidulans中的異源表達,ii)基因terABC在A(yíng). nidulans中的異源表達;(D)蛋白TerC的體外反應:(i)蛋白TerC將底物32轉化為2,(ii)煮沸過(guò)的TerC對底物32失活,(iii)蛋白TerC對底物33無(wú)反應;(E)蛋白TerB的體外反應:(i)微粒體蛋白TerB可以催化底物25轉化為32,(ii)蛋白TerB和TerC可以將25轉化為2;(F)Terrecyclic acid (2)的生物合成途徑。
在發(fā)現新型倍半萜環(huán)化酶(β-terrecyclene合酶,TerA)可以催化法尼基焦磷酸(FPP)轉化為β-terrecyclene(25)的基礎上,通過(guò)對TerA的系列定點(diǎn)突變研究(圖3),結合動(dòng)力學(xué)同位素效應分析(圖4),確證了環(huán)化過(guò)程為Coates途徑,而非最早提出的Hirota途徑。
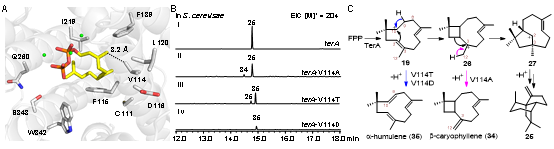
圖3?基因terA的點(diǎn)突變、產(chǎn)物及其機制
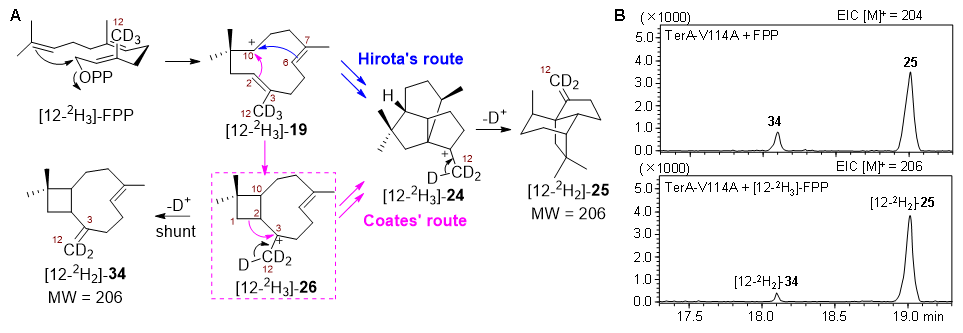
圖4?突變株TerA-V114A的動(dòng)力學(xué)同位素效應 (A) 通過(guò) [12-2H3]-FPP 的動(dòng)力學(xué)同位素效應區分Hirota和Coates途徑. (B) FPP和[12-2H3]-FPP 為底物比較TerA-V114A產(chǎn)物的動(dòng)力學(xué)同位素效應。
通過(guò)以上研究,作者發(fā)現了抗菌、抗腫瘤quadrane骨架倍半萜terrecyclic acid的生物合成基因簇,以此為基礎,解析了其通過(guò)β-terrecyclene環(huán)化酶TerA形成quadrane骨架,繼而氧化、脫氫的后修飾的生物合成過(guò)程。Quadrane骨架的形成機制也通過(guò)對蛋白TerA的點(diǎn)突變和動(dòng)力學(xué)同位素效應得以證實(shí),從而解決了幾十年來(lái)關(guān)于該類(lèi)天然產(chǎn)物生物合成研究的謎團。該研究也為進(jìn)一步以萜類(lèi)環(huán)化酶TerA為探針,從真菌數據庫中對quadrane類(lèi)天然產(chǎn)物的發(fā)掘奠定了基礎。
以上研究,副研究員宋永相為第一作者,研究員閆巖為通訊作者。由濟南大學(xué)的王文貴博士,美國加州大學(xué)洛杉磯分校(UCLA)唐奕(Yi Tang)教授團隊合作完成。
上述研究工作得到了國家重點(diǎn)研發(fā)計劃、海南省科技計劃三亞崖州灣科技城科技創(chuàng )新聯(lián)合項目、國家自然科學(xué)基金、中國科學(xué)院王寬誠率先人才計劃“盧嘉錫國際團隊項目”和海南省自然科學(xué)基金、廣東特支計劃?“海洋藥物研究開(kāi)發(fā)創(chuàng )新團隊”等的資助。
Chemical Science作為英國皇家化學(xué)會(huì )資助的旗艦期刊,對各國研究人員在化學(xué)領(lǐng)域取得的突破性成果,經(jīng)評審接收后免費發(fā)表,并對全球讀者開(kāi)放獲取。文章接收后,被Chemical Science評為每周亮點(diǎn)論文(2024 ChemSci Pick of the Week Collection)和2024熱點(diǎn)論文(2024 Chemical Science HOT Article Collection)。
本文鏈接:https://pubs.rsc.org/en/content/articlelanding/2024/sc/d4sc01208a。
文章相關(guān)信息:Yongxiang Song,Wengui Wang,Jiafan Yang,De-Wei Gao,John M Billingsley,Songtao Wang,Yiguang Zhu,Junfeng Wang,Jianhua Ju,Yan Yan* and Yi Tang. Chem. Sci.,2024,doi.org/10.1039/D4SC01208A
附件下載:


